진행성 위 및 위식도 접합부 선암 환자에서
| 최근 진행성 위 및 위식도 접합부 선암에서 2차 항암화학요법 치료로 세포독성 항암제 또는 분자표적치료제를 단독 또는 병용해 사용하는 임상시험들이 활발히 진행돼 그 결과가 발표되고 있다.(1)
2014년 9월 란셋 온콜로지(Lancet Oncology)에 게재된 RAINBOW 임상시험은 진행성 위 및 위식도 접합부 선암 환자에서 2차 항암화학요법으로 진행된 가장 큰 규모의 연구이며, 기존 항암화학요법과 VEGFR-2 표적 항체를 병용해 생존율 증가를 보고한 최초의 임상시험이라는 점에서 의의를 갖는다. |
라무시루맙은 혈관내피세포성장인자 수용체-2(이하 'VEGFR-2')에 특이적으로 결합하는 인체면역글로불린G1(IgG1) 단일클론항체로, VEGFR-2에 결합해 VEGF 수용체 리간드인 VEGF-A, VEGF-C 및 VEGF-D의 수용체 결합을 차단한다.

라무시루맙을 통해 VEGFR-2의 활성화가 저해되면, 리간드 유도 세포 증식과 혈관내피세포의 이동 및 암세포의 혈관생성 관련 신호전달과정을 억제할 수 있다.(2)
이 연구는 진행성 위 또는 위식도 접합부 선암 환자 중, 1차 항암화학요법 치료 후 질병이 진행된 환자를 대상으로 VEGFR-2에 대한 단일클론항체 길항제인 라무시루맙을 파클리탁셀과 병용 투여하였을 때 전체 생존기간 개선에 미치는 효과를 위약과 파클리탁셀 병용 투여와 비교 평가했다.
이 연구는 라무시루맙과 파클리탁셀의 병용요법이 진행성 위 및 위식도 접합부 선암 환자의 2차 치료에서 새로운 표준요법으로 사용될 수 있는 지를 검증하기 위해 시행됐다.
시험 방법
RAINBOW 임상시험은 이중 맹검·위약대조·3상 연구로 VEGFR-2 길항제인 라무시루맙과 파클리탁셀 병용의 유효성 및 안전성을 검증하고자 2010년 12월 23일부터 2012년 9월 23일까지, 665명의 연구대상자를 라무시루맙과 파클리탁셀군(330명) 또는 위약과 파클리탁셀군(335명)으로 무작위 배정해 진행했다.
이 연구는 1차 요법으로 플루오로피리미딘과 백금화합물을 병용한 항암화학요법 도중이나 이후 질병이 진행된 18세 이상 전이성 또는 절제불가능한 국소진행성 위 또는 위식도 접합부 선암 환자를 대상으로 했다.
임상시험은 북미·남미·유럽·아시아·오스트레일리아 등 27개국의 170 기관에서 진행됐으며 양 군 간 베이스라인 인구학적 및 임상 특성은 차이가 없었다.
치료의 유효성을 판단하는 기준으로 일차 평가변수로는 전체생존기간을 보았고, 2차 평가변수로 무진행생존기간을 비롯해 종양 반응률·질병 조절률(disease control rate)과 삶의 질 및 안전성을 비교했다.
시험 결과
연구종료시점인 2013년 7월 12일 기준으로 모든 환자의 전체생존기간 중앙값은 7.9개월(IQR 4.2~13.0)로 관찰됐다. 라무시루맙과 파클리탁셀 병용군(이하 '라무시루맙군')에서 위약과 파클리탁셀 병용군(이하 '대조군')과 비교해 전체 생존기간과 무진행 생존기간이 모두 통계적으로 유의하게 증가됐고, 반응률 및 질병 조절률 역시 라무시루맙군에서 우월했다.
▶라무시루맙 치료의 전체 생존기간 개선
본 연구에 참여했던 환자들 중 라무시루맙군의 중앙 전체생존기간은 9.6개월(95% 신뢰구간 [CI] 8.5~10.8)로 대조군의 7.4개월(95% CI 6.3~8.4)과 비교해 유의한 연장을 보였다(위험비 [HR] 0.807, 95% CI 0.678~0.962, p=0.017) (그림 1).
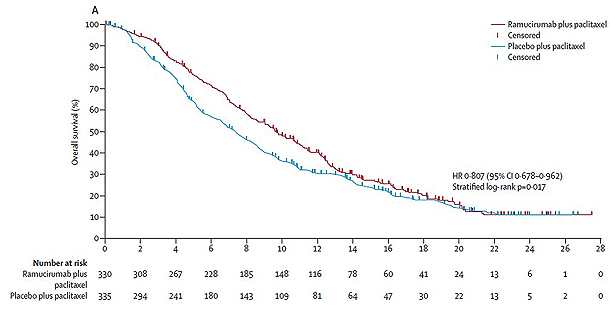
또한 12개월 전체생존율 역시 라무시루맙군에서 40%(95% CI 35~45)로, 대조군의 30%(95% CI 25~35) 보다 개선됨을 관찰할 수 있었다.
라무시루맙군의 중앙 무진행생존기간 또한 4.4개월(95% CI 4.2~5.3)로 대조군의 2.9개월(95% CI 2.8~3.0)과 비교해 유의한 연장을 보였다(HR 0.635, 95% CI 0.536~0.752, p<0.0001) (그림 2).

6개월과 9개월 무진행 생존율 역시 라무시루맙군에서 대조군 보다 각각 19%, 12%의 증가를 보였다.
라무시루맙군에서 종양 반응률은 28%(95% CI 23~33)으로 대조군의 16%(95% CI 13~20)에 비해 유의하게 높았다(p=0.0001). 질병 조절률 역시 라무시루맙군에서 대조군에 비해 유의하게 높았다(80% vs 64%, p<0.0001).
▶라무시루맙 치료의 안전성 결과
중증도, 즉 3도 또는 4도의 이상반응의 발생률은 라무시루맙군에서 대조군에 비해 높았으나, 치료 중단이나 사망률을 높이는 결과로 이어지지 않았으며, 라무시루맙으로 치료 받는 동안 환자들의 삶의 질은 잘 유지되는 결과를 관찰할 수 있었다.
VEGF 경로와 잠재적으로 연관돼 있는 이상반응으로 3도의 고혈압·단백뇨·출혈은 라무시루맙 군에서 더 흔하게 발생했다. 4도 또는 5도의 중증 고혈압은 발생하지 않았으며, 4도 또는 5도의 위장 출혈은 양 군에서 모두 유사하게 낮았고, 위장관 천공은 라무시루맙군에서 대조군보다 약간 높았으나 1% 미만의 낮은 빈도로 관찰됐다.
피로·설사·복통은 양 군 모두에서 가장 흔하게 보고된 비혈액학적 이상반응으로 라무시루맙군에서 더 흔하게 발생했다. 그러나 이러한 이상반응들은 위암 환자에서 일반적으로 발생할 수 있으며, 본 임상시험에서의 발생률은 이전에 시행된 대규모 위암 3상 임상시험에서 보고된 발생률 범위 안에 있었다.
말초신경병증은 taxane계 항암제의 전형적인 부작용으로 라무시루맙군에서 발생률이 조금 더 높았으나 이는 파클리탁셀의 누적 용량과 관련이 있었다.
3도 이상의 호중구감소증은 양 군에서 가장 빈번하게 발생한 혈액학적 독성으로 라무시루맙군에서 역시 높게 관찰됐으나 임상적으로 의미 있는 발열성 호중구감소증은 양 군 간 차이가 없었다.
논의 및 결론
RAINBOW 임상시험은 현재까지의 연구 중 진행성 위 및 위식도 접합부 선암의 2차 치료에서 가장 큰 규모로 시행된 연구이며 항암화학요법과 병용한 VEGFR-2 표적 항체에 의한 생존율 향상을 보고한 최초의 보고로서 VEGFR-2 표적 항체를 통해 진행성 위암 환자들의 전체생존기간을 유의하게 향상시킬 수 있음을 증명했다는 점에서 의의가 있다.
본 연구에서 파클리탁셀과 라무시루맙 병용 사용군의 전체생존기간의 중앙값이 9.6개월로 파클리탁셀과 위약 대조군 대비 중앙값 2.2개월의 생존기간 연장이 유도됐다.
진행성 위암의 2차 치료 상황에서 최적의 지지요법에 의한 생존기간이 3~4개월에 불과한 점을 고려했을 때, 파클리탁셀과 라무시루맙 병용요법은 최적의 지지요법 대비 총 4개월 이상의 생존 연장 효과를 보였다고 할 수 있다.(1)-(7)
결론적으로, 본 연구는 진행성 위암 환자들에서 라무시루맙과 파클리탁셀의 병용요법이 새로운 표준 2차 항암화학요법으로 사용될 수 있음을 제시했다고 할 수 있다.
|
(1) Se Hoon Park, Soon Il Lee. Recent Advances in Chemotherapy of Gastric Cancer.The Korean Journal of Medicine. Vol.82, No 4, 2012 |
* 본 페이지는 한국릴리의 후원으로 기획했으나 기사내용은 회사와 무관합니다


