
대한심장학회 혈관연구회(회장 박정배)는 지난 4월 17일 대한심장학회 춘계 심포지엄 강연차 한국을 방문한 Louis J. Ignarro 교수(UCLA School of Medicine/1998년 노벨생리의학상 수상)와 '심혈관질환에서 산화질소(NO:Nitric Oxide)의 역할'을 주제로 학술좌담회를 열었다.
특히 이날 좌담회에서는 혈관내피세포 기능을 보존하고, NO 분비를 통해 혈관을 이완하는 특성을 지닌 Nebivolol이 기존의 베타차단제와 어떤 차이가 있는지에 대한 논의도 진행됐다. <의협신문>은 이날 발표된 내용을 지면을 통해 소개한다.<편집자주>
| 기체성 신호전달분자인 산화질소(NO)의 발견과 발전사 |
NO의 약리학적 효과 발견

NO에 대한 연구는 1970년대말 Ferid Murad 박사(1998년 노벨생리의학상 공동수상자)가 세포 내 cGMP 생성을 촉진하는 효소인 guanylate cyclase를 NO가 활성화시키는 것을 우연히 발견하면서 시작됐다. 하지만 당시에는 세포 내에서 cGMP의 역할조차 알지 못했다. 이 연구에서 NO를 cGMP를 증가시키는 도구로 사용했고, cGMP가 비혈관 평활근을 이완시키는 것을 발견했다.
또 다른 의문은 혈관확장제로 사용되는 nitroglycerin의 작용기전이었다. Nitroglycerin은 1870년대부터 협심증(angina) 치료제로 사용돼 왔다. Nitroglycerin의 혈관확장 효과는 nobel 다이너마이트 공장에서 처음 발견됐는데 nitroglycerin이 공장에 근무하던 노동자의 협심증 통증을 완화시켰던 것이다. 하지만 그 기전은 100여 년이 지난 후에야 밝혀졌다.
Murad 박사는 nitroglycerin의 nitro-(NO2-)기 중 하나가 NO로 전환되고, 이로 인해 nitroglycerin이 혈관확장 효과를 갖는다는 가설을 세웠으며, 1980년 실험을 통해 이 가설이 사실임을 확인했다. 동맥평활근에 nitroglycerin을 주입하자 NO가 생성됐다.
가스 상태의 순수 NO를 소의 관상동맥에 주입하자 혈관평활근이 이완되는 것이 관찰됐다. 여기에 NO를 파괴하는 헤모글로빈이나 methylene blue를 추가하면 이완 효과가 차단됐다. 가설대로 NO가 혈관확장 성분임을 확인할 수 있었다. 또 이완이 시작되기 1~2초 전에 cGMP 증가가 관찰돼 cGMP가 NO의 혈관확장의 매개체 역할을 한다는 것이 입증됐다.
또 NO가 혈소판에 미치는 영향도 확인했다. Sodium Nitroprusside의 혈소판 응집 억제 효과가 NO에 의한다는 가설 하에 실험을 했다.
실험 결과 ADP(adenosine diphosphate)로 유도한 혈소판 응집을 NO가 억제한다는 것이 최초로 밝혀졌다.
이 같은 연구를 통해 1980년 NO의 약리학이 밝혀졌다. NO는 혈관평활근 이완·혈관확장·고혈압환자의 혈압 강하 및 혈류 개선 효과가 있고, 혈소판 응집을 억제해 혈전을 억제하는 효과가 있음이 밝혀졌다. 하지만 여전히 NO와 cGMP 간의 생리학적 연관성은 밝혀지지 않았고, NO가 체내에서 자연 생성되는 신호전달분자(signaling molecule)라는 생각은 하지 못했다.
NO의 내생 가능성과 EDRF
cGMP는 세포 내에 존재하며 NO에 대한 guanylate cyclase의 높은 민감성이 증명됐기 때문에 NO가 체내에 없다면 cGMP가 왜 체내에 있는지 의문을 갖게 됐다.
NO가 체내에서 생성되는데 아무도 밝혀내지 못한 것이 아닐까라는 의문을 갖게 됐지만 NO의 화학적 속성을 검토한 후 NO의 내생 가능성이 낮다는 결론에 도달했다.
첫째, NO는 작은 지용성 분자이다. 둘째, NO는 세포막을 통해 빠르게 분산되기 때문에 세포기관에 저장되지 않는다. 셋째, NO는 반감기가 아주 짧은 free radical이다. 대기 중 NO의 반감기는 1초가 채 되지 않는다. 넷째, NO는 다른 상자성(paramagnetism) 종을 찾고 활성산소와 반응한다. 또 철 및 유황과도 반응한다.
이처럼 NO의 내생 가능성을 부정하는 수많은 자료에도 불구하고 NO가 체내에 존재한다는 확신을 가졌다. NO를 필요로 하는 cGMP가 체내에 분명 존재하기 때문이다.
그래서 체내에서 NO를 찾기 위해 연구를 진행했는데, 결국 실패했다. 그런데 1980년 Robert F. Furchgott (1998년 노벨생리의학상 공동수상자)가 acetylcholine이 혈관내피에서 이완인자의 생성을 촉진해 혈관을 이완시킨다는 것을 알아냈고, 이 미지의 이완인자를 EDRF(endothelium-derived relaxing factor)라고 명명했다.
Furchgott의 연구결과를 바탕으로 cGMP를 측정하는 실험을 진행하게 됐다. 혈관평활근에 acetylcholine을 투여한 후 cGMP를 측정한 결과, acetylcholine에 의해 cGMP가 유의하게 증가하고 이로 인해 혈관평활근이 이완되는 것이 밝혀졌다. Methylene blue를 추가해 cGMP 생성을 억제하자 acetylcholine을 투여해도 혈관평활근이 이완되지 않았기 때문이다.
이는 몇 년 전 NO를 사용한 실험과 동일한 결과였다. 당시에도 NO가 내피 독립적인 이완물질을 배출해 cGMP를 증가시켜 혈관평활근을 이완시켰고, 이 이완 효과는 methylene blue를 추가하면 차단됐다.
이처럼 EDRF와 NO 사이에는 놀라울 정도의 공통점이 있었다. EDRF와 NO는 모두 cGMP를 증가시키고, 혈관확장을 위해 cGMP를 필요로 했다. EDRF가 NO일 수도 있다는 가설이 나왔고 일련의 연구가 진행됐다. 당시 많은 학자들이 EDRF를 분리 수집하기 위해 노력했으나 EDRF가 너무 불안정해 성공하지는 못했다.
하지만 NO에 적용했던 방법을 EDRF에 적용해 EDRF를 안정화, 분리 및 수집하는 데 성공했고, 그 결과 1986년에 EDRF가 바로 NO인 것을 증명할 수 있었다.
또 acetylcholine을 비롯한 내피종속적 혈관확장제의 작용 기전을 밝힐 수 있었다.
신호전달분자 NO
NO의 화학적 속성을 처음 검토했을 때 NO는 신호전달분자일 수가 없다는 결론에 도달했다. 하지만 NO가 EDRF라는 사실을 바탕으로 NO의 화학적 속성을 다시 보면 정반대의 결론이 나온다. 첫째, NO는 작은 지용성 분자이고 세포막을 통해 빠르게 분산된다. 따라서 완벽한 신호전달분자가 될 수 있다.
둘째, NO는 다른 free radical 및 활성산소에 반응한다. Superoxide와 같은 free radical은 NO의 작용을 중단시키며, NO와 같은 신호전달분자의 작용이 오래 지속될 필요는 없다. 또한 신호를 생성한 분자는 사라지는 것이 맞다. 셋째, NO는 철 및 유황 종과 반응한다.
앞서 말했듯 NO는 guanylate cyclase를 활성화 하는데 NO가 guanylate cyclase의 철과 결합하기 때문이다.
이 연구결과가 발표되자 여러 분야의 학자들이 NO를 연구하기 시작했고, NO가 심혈관 뿐만 아니라 신경전달·항염증·숙주방어·위장·폐·비뇨생식 등에도 중요한 역할을 한다는 것이 밝혀졌다. NO가 혈관 내에서 생성될 수 있음이 증명된 후 수많은 획기적인 발전이 이루어진 것이다.
NO는 NO synthase에 의해 세포 내에 생성된다. 반응의 기질은 아미노산 중 하나인 arginine이다.
Arginine의 아미노기 중 하나가 NO synthase에 의해 N-hydroxiyarginine로 변환된 후 다시 산화 및 정화되어 NO가 생성된다. 이 NO synthase 반응에서 나오는 두 번째 산물이 citrulline이다. Citrulline은 신장뿐 아니라 내피세포에서 다시 arginine으로 변환되고 따라서 다시 NO가 생성되는 과정이 반복된다.
신경전달물질 NO : 발기능(erectile function)의 매개체
1990년 발기에 작용하는 신경전달물질(neurotransmitter)에 대한 의문에서 발기능에 대한 NO의 영향을 연구하게 됐다. NO는 세포막과 조직을 통해 쉽게 분산되고 천천히 이완작용을 일으킬 수 있다. 발기 시 혈관이 확장되는 것에 착안해 NO가 발기능을 매개하는 신경전달물질이라는 가설을 실험했다.
토끼의 음경해면체(corpus cavernosum)를 이용한 첫 번째 실험에서 이 가설이 사실임이 바로 입증됐다. 이후 1992년 인간의 음경해면체를 이용해 NO가 발기능을 매개하는 신경전달물질임을 증명했다.
6년 후인 1998년 Pfizer는 cGMP와 NO의 작용을 증가시키는 발기부전 치료제 sildenafil(Viagra)를 발매했고, 나는(Ignarro 박사) NO의 신호전달체계에 대한 연구로 그 공로를 인정받아 1998년 노벨생리의학상을 공동 수상하게 됐다.
NO의 치료 효과
북남미·유럽·아시아를 비롯해 전세계적으로 이환율과 조기사망의 가장 큰 원인은 심혈관질환이다. 내피세포를 건강하게 유지하지 못하면 NO가 충분히 생성되지 않는 내피세포 기능부전(endothelial dysfunction)이 발생한다.
내피세포 기능부전은 고혈압·국소 혈류장애·발기부전·제2형 당뇨병 증상·혈액순환 저하로 인한 만성 사지통증·죽상경화증 등을 유발한다. 그 중 죽상경화증(atherosclerosis)은 염증성질환이다. NO의 혈관확장 작용이 주로 강조되지만 NO는 항염증 속성이 있는 강력한 항산화제이기도 하다.
즉, NO는 혈소판·호중구(neutrophil) 및 단핵구(monocyte)가 혈관 내막의 표면에 쌓이지 않도록 하여 혈소판 응집과 죽상경화증을 방지한다. 따라서 NO를 생성하는 내피세포층을 건강하게 유지하는 것이 매우 중요하다.
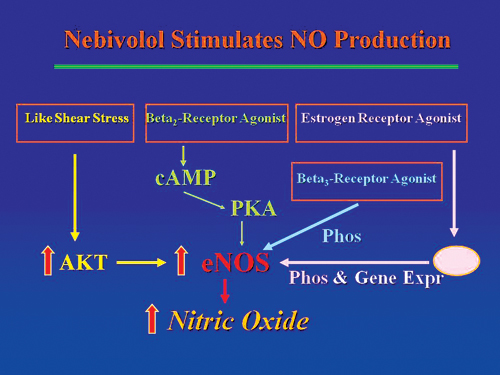
NO로 심혈관질환을 예방하는 Nebivolol
심혈관질환에 NO를 활용한 대표적인 약제 중 하나가 nebivolol이다. Nebivolol은 심장의 베타-1 아드레날린수용체에 대한 선택성이 매우 높은 베타차단제이자 혈관확장제이다. 베타차단제 중 혈관은 확장시키지만 수용체 대항제 역할을 하지 않는 제품은 많다.
하지만 eNOS(endothelial NO synthase)를 자극해 NO의 생성을 증가시킴으로써 혈관확장 효과를 증대시키는 베타차단제는 Nebivolol이 유일하다.
MENARINI와 UCLA는 nebivolol에 대한 공동연구를 진행했다. 먼저 쥐의 대동맥으로 실험한 후 인간의 동맥조직에도 동일한 실험을 진행했고 동일한 결과를 얻었다.
쥐의 대동맥으로 내피 종속적 이완과 내피 비종속적 이완을 실험했는데 nebivolol은 주로 내피종속적 이완을 유발했고 약간의 내피비종속적 이완도 유발했다. 인간 조직을 대상으로 한 시험에서 내피가 없을 때 nebivolol은 이완을 전혀 유발하지 않았다.
또 쥐 실험에서 eNOS를 억제하는 NMA(N-methyl arginine)를 추가하자 nebivolol의 이완 효과가 감소했다. NO를 파괴하는 헤모글로빈과 cGMP 생성을 억제하는 ODQ를 추가했을 때도 nebivolol의 이완 효과가 감소했다. 반면 cGMP를 축적시키는 ZAP은 nebivolol의 이완 효과를 증대시켰다.
쥐의 대동맥 평활근세포(SMC, smooth muscle cell)로 nebivolol이 혈관평활근에 미치는 영향을 조사한 결과 nebivolol이 SMC 증식을 억제하는 것으로 나타났다. 반면에 atenolol은 전혀 영향을 미치지 않았다. 이와 같은 nebivolol의 SMC 증식 억제 기전은 arginine에서 시작된다.
Arginine은 NO뿐 아니라 세포성장을 담당하는 polyamine도 생성한다. Nebivolol과 arginine에 의해 생성된 NO가 ODC(ornithine decarboxylase)와 결합한다. 또한 NO는 sulfur에 반응하는데, ODC의 SH기(sulfur hydro group)와 NO가 결합하는 것이다.
이렇게 ODC가 억제되면 putrescine과 polyamine이 생성되지 않아 세포가 성장되지 않는다. Nebivolol 투여 후 putrescnine, ODQ 및 zaprinast를 추가한 후속 실험에서 NO와 nebivolol에 의한 세포증식 억제효과는 cGMP에 의해 매개되지 않는다는 것을 알아냈다.
결론적으로 nebivolol의 고유한 특성을 정리하면, 첫째, NO를 매개로 혈압을 강하시키는 동시에 베타차단제로서 작용을 해 심장을 보호한다. 둘째, NO를 매개로 혈전증(thrombosis)을 예방 또는 감소시킨다. 셋째, NO를 매개로 죽상경화증(atherosclerosis)을 예방한다. 넷째, 심부전을 예방한다.
| 각종 혈관확장 베타차단제 프로파일과 Nebivolol역할 |
베타차단제 발전사

3세대 베타차단제: Carvedilol vs Nebivolol
Carvedilol은 베타차단 효과에 알파차단 효과를 더했다. 즉, 알파차단 효과로 혈관의 혈관확장을, 베타-1에 대한 선택성이 있는 베타차단 효과로 심장의 혈관확장을 담당하게 한 것이다. 반면 nebivolol은 베타-1에 대한 선택성은 유지하되, 새로운 기전인 NO로 인한 혈관확장 기능을 이용했다.
Nebivolol은 2개의 거울상 이성질체인 D-nebivolol과 L-nebivolol로 나뉜다. D-nebivolol은 기존 베타차단제와 마찬가지로 심박수를 감소시킨다. 대신 L-nebivolol이 생성한 NO의 혈관확장 효과로 인해 말초관류가 늘어나고 따라서 심박수가 다시 정상화된다.
Nebivolol의 약리역학
임상에서 가장 중요한 문제는 nebivolol을 신장이 안좋은 환자에게 처방할 수 있는가이다. nebivolol은 소변으로 38%, 대변으로 48%가 배출된다.
또 nebivolol은 혈장단백결합률이 98%이다. 따라서 nebivolol은 결합된 단백질이 서서히 배출돼 베타차단제 중에서 반감기가 가장 크고, 그 결과 1일 1회만 투여하면 된다. 반면에 atenolol은 약효가 24시간 지속되지 않아 뇌졸중 방지 효과가 적다는 단점이 있다.
베타차단제 중 가장 많이 사용되는 carvedilol의 단점은 베타-1 선택성이 낮다는 것이다. 한국은 물론 전세계 심부전 환자의 절반 정도가 HFpEF(heart failure with preserved ejection fraction: 좌심실 구혈률이 유지되는 심부전) 환자이고, 이들 중 상당수가 COPD(Chronic Obstructive Pulmonary Disease: 만성폐쇄성폐질환)을 갖고 있다.
COPD 환자에게 Aarvedilol을 투여하면 베타-1 선택성이 없어 천식이 악화될 수 있다. 따라서 천식 위험이 있는 노인 COPD 환자의 경우 Nebivolol의 베타-1 선택성은 아주 큰 장점이다.
Nebivolol의 항혈전 기능
2014년 ATBV에 발표된 연구자료에 따르면 nebivolol은 폐혈전색전증에 의한 사망률을 감소시킨다. 이 연구에서는 에피네프린 유도 폐혈전색전증(epinephrine-induced pulmonary thromboembolism)에 걸린 쥐에게 nebivolol을 투여했다.
야생형 쥐들의 경우 nebivolol 투여군과 비투여군의 생존율이 20% 대 60%로 차이가 났고, eNOS-/- 유전자제거 쥐의 경우 전혀 차이가 없었다.
특히 L-nebivolol/DL-nebivolol 투여군의 경우 사망률이 대폭 감소했으나, eNOS-/- 쥐에서는 전혀 차이가 없었고, D-nebivolol과 bisoprolol 투여군은 사망률 감소 효과가 전혀 보이지 않았다.
연구진은 L-nebivolol의 eNOS 종속적 효과가 에피네프린 유도 폐혈전색전증에 대한 방어효과가 있다고 보았다. 혈소판 활성화에 미치는 영향을 확인하기 위해 혈소판 표면마커인 P-selectin 발현을 조사했다. 야생형과 eNOS-/- 쥐들 모두 에피네프린을 자극하면 P-selectin이 많이 발현된다.
L-nebivolol 투여시 P-selectin 발현, 즉 혈소판 활성화가 일어나지 않는다. 반면 eNOS-/- 쥐와 D-nebivolol 투여군에서는 전혀 이런 방어효과가 보이지 않는다. 따라서 혈소판 활성화의 방어효과는 베타-1이 아닌 eNOs가 매개된 효과라는 것을 알 수 있다.
또 이 연구에서는 혈소판내 cGMP 수치와 혈소판유래 NOx를 조사했다. L-nebivolol은 eNOS- 쥐가 아닌 쥐에서 cGMP를 증가시키고 혈소판 내 NOx 농도 역시 증가시켰다.
결론적으로 nebivolol 투여시 생존률이 증가하고 혈소판 활성이 감소한다. 혈소판 활성을 감소시키는 것이 NO인데 Nebivolol에 의해 NO가 증가한 것이다.
Nebivolol의 지질분해 기능
보통 베타차단제 투여시 살이 찌고 중성지방이 증가한다. 이 문제를 논의하려면 지방대사에서 b3AR(beta3-adrenergic receptor: 베타3 아드레날린 수용체)의 역할을 이해할 필요가 있다. b3AR는 관상동맥내피에서 NO 생성을 증가시키고, 심근에서는 NO와 cGMP를 생성해 수축성을 감소시킨다. 중요한 것은 지방세포에서의 역할이다.
b3AR는 지방을 태우는 역할을 한다. 기온이 낮으면 교감신경 활성도와 b3AR 발현이 증가한다. 즉, 추울 때 땀을 만들어 체온을 유지시키는 것이 b3AR이라고 추정된다. 특히 b3AR은 갈색지방세포의 열 발생에 중요한 역할을 하는 것으로 보인다.
피하 및 내장 지방세포를 보면 지방방울이 있다. Nebivolol을 투여하면 이 지방방울의 직경이 감소한다. L-nebivolol 투여 시 지방분해가 증가하지만 D-nebivolol 투여 시 증가하지 않는다. b3AR 작용제인 BRL(BRL37344)을 투여하면 지방분해가 증가한다.
반면 nebivolol과 b3AR 대항제인 SR(SR59230A)을 함께 투여하면 지방분해 효과가 감소한다. b3AR 작용제를 차단하면 지방분해 효과가 없어지는 것이다. 따라서 지방분해는 b3AR에 의한 것이고, nebivolol은 이 b3AR를 자극하는 효과가 있다고 볼 수 있다.
Nebivolol의 고혈압 치료 효과
고혈압 약제에서 가장 중요한 점은 24시간 약효가 지속되는가이다. 그 지표가 되는 것이 T/P(trough-to-peak ratio)이다. T/P가 100%이면 전날 약을 먹고 다음날 먹기 전까지 약효가 유지된다는 뜻이다. Atenolol은 T/P가 낮아 새벽에 약효가 떨어진다는 단점이 있다. 반면 nebivolol은 T/P가 89%로 1회 투여로 24시간 약효가 유지된다.
각종 연구를 통해 항고혈압 효능 면에서 nebivolol은 atenolol과 유사하고, metoprolol보다 우수한 것으로 나타났다. 또한 항고혈압제인 losartan보다 우수하고, amlodipine과 유사하다.
경미한 본태성 고혈압환자를 대상으로 순수 베타-1 선택제제인 bisoprolol을 비교한 결과 nebivolol은 말초혈관의 혈관확장 효과가 우수해 SVR(Systemic Vascular Resistance: 전신혈관저항지표)이 감소했다.
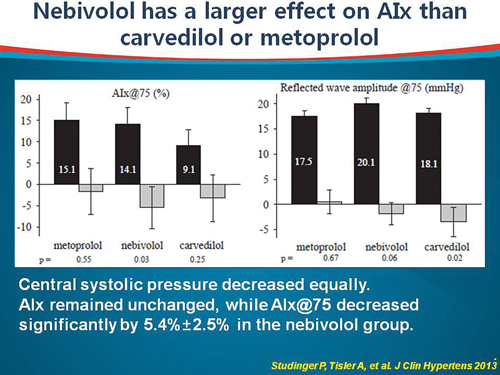
특히 nebivolol은 중심혈압을 낮추는 데 큰 효과를 볼 수 있다. Metoprolol과 비교할 때 nebivolol은 중심 수축기/이완기혈압이 모두 감소하고, 중심맥압(central pulse pressure)도 감소한다는 장점이 있다. 2013년 한 연구에서 반사파진폭(reflected wave amplitude)의 영향을 조사했다.
AI(Augmentation Index)를 보면 nebivolol과 carvedilol 모두 metoprolol에 비해 감소했다. 베이스라인 지정에 논란이 있긴 했지만 말초혈관을 확장시키는 nebivolol과 carvedilol이 metoprolol보다 AI를 감소시키는 데 더 효과가 있는 것을 알 수 있다.
흥미로운 점은 carvedilol은 심박수 변화에 따라 AI 감소 정도가 다르다는 것이다. 즉, 심박수가 떨어지지 않으면 AI 변동이 많고, 심박수가 떨어지면 AI 변동이 적다. 반면 nebivolol은 심박수의 영향을 받지 않았다.
Nebivolol의 안전성
심부전에 가장 널리 사용되는 것은 carvedilol이다. 그러나 통계를 보면 고령의 심부전 환자 중 1/3 이상이 COPD를 갖고 있다.
이런 환자에게 과연 비선택적 베타차단제를 써도 되는가? 그러나 nebivolol의 경우, COPD가 있는 고혈압 환자에게 nebivolol과 위약을 투여했을 때 FEV1이 감소되지 않았다는 연구 결과가 발표된 바 있다(Cazzola M et al. Respiration 2004 Mar-Apr;71(2):159-64 참조).
또 nebivolol은 고혈압 환자의 발기부전 치료에도 효과를 보였다(Doumas M et al. Asian J Androl 2006;8:177-82 참조). atenolol, bisoprolol 또는 metoprolol을 투여하던 고혈압환자에게 nebivolol을 처방한 결과 발기부전을 호소한 환자가 줄었다. 베타차단제를 투여하는 고혈압 환자에게 발기부전이 있을 때 nebivolol로 바꾸면 발기부전을 상당히 호전시킬 수 있다.
Nebivolol은 간헐성 파행(Intermittent Claudication)과 동맥성 고혈압(Arterial Hypertension)을 앓고 있는 환자에게도 효과가 있었다(Espinola-Klein C et al. Hypertens 2011;58(2):148-54 참조). Metoprolol 투여 시 파행거리(claudication distance)에 변화가 없었으나 nebivolol 투여시 시간이 갈수록 파행거리가 증가했다.
지질대사 악화는 베타차단제의 가장 큰 단점이다. 비선택적 베타차단제는 혈장중성지방과 LDL 콜레스테롤을 증가시킨다.
선택적 베타차단제인 atenolol 역시 지질대사를 악화시킨다. 여러가지 요인이 있지만, 주된 원인은 베타차단제가 포도당과 콜레스테롤, 즉 칼로리를 소비하는 주 기관인 근육으로 가는 혈류를 감소시키기 때문이다.
Atenolol과 비교 시 혈관확장 기능이 있는 nebivolol은 LDL-콜레스테롤 감소 효과가 뛰어나고, 특히 중성지방을 크게 감소시킨다(Pesant Y, et al. Am J Ther 1999; 8:283-8 참조).
기존 베타차단제는 당뇨를 새로 발병시키는 문제가 있었으나 nebivolol 투여시 새로 당뇨가 발병하지 않았다. 2006년 고혈압환자 6000명을 대상으로 Nebivolol의 유해사례를 조사한 결과 우울증·구역 및 불임 발생률이 놀라울 정도로 낮았다(Cleophas TJ, et al. Am J Therap 2006; 13:192-7 참조).
결 론
기존 베타차단제와 혈관확장 베타차단제는 혈류역학에서 차이가 있다. 1세대 및 2세대 베타차단제는 혈압과 심박수는 감소시키지만 말초저항을 증가시킨다. 그로 인해 포도당과 콜레스테롤을 소비하는 근육으로 가는 혈류량을 감소시켜 지질대사에 악영향을 미친다.
2세대 베타차단제인 atenolol과 metoprolol의 가장 큰 단점이 바로 이 점이다. 반면 3세대 베타차단제는 혈관확장 기능을 갖고 있기 때문에 말초저항을 감소시킨다.
결론적으로 3세대 베타차단제 Nebivolol의 장점을 정리하면 첫째, nebivolol은 혈관을 확장시키기 때문에 지질대사에 영향을 주지 않는다. 둘째, nebivolol은 베타-1 선택성이 높기 때문에 COPD 환자에게도 투여가 가능하다. 셋째, nebivolol은 혈소판 활성을 유의적으로 감소시킨다.
넷째, nebivolol은 발기부전을 개선시킨다. 베타차단제 투여 중 발기부전을 호소한 환자에게 nebivolol을 처방한 결과 50% 정도의 환자에서 발기부전이 감소했다. 다섯째, nebivolol은 운동능력에 영향을 미치지 않는다. 운동능력은 심박출량(cardiac output)의 영향을 받는다.
Nebivolol은 심박수를 감소시키지만 혈관확장을 통해 운동능력을 유지시킨다. Nebivolol은 이 같은 장점이 있는 동시에 부작용이 적기 때문에 베타차단제를 필요로 하는 환자 중 특히 노인환자와 천식·비만 및 발기부전을 동반한 환자에게 효과가 있을 것으로 본다.
|
< 패널토의 > ▶성기철 : Nebivolol의 혈소판 응집 억제 효과에 대해 질문하겠다. 실제 임상에서 아스피린처럼 뇌졸중을 예방하는 효과가 있는가? 일반 베타차단제에 아스피린을 처방하는 것보다 nebivolol에 아스피린을 추가 처방하는 것이 효과적이라고 할 수 있는가? ▶이해영 : 항혈소판제로 아스피린과 일반 베타차단제를 같이 처방하는 경우는 있어도 베타차단제만 처방하는 경우는 없다. 다만, 아스피린에 일반 베타차단제를 더하는 것보다 아스피린에 nebivolol을 더하는 것이 더 효과가 크다고 볼 수 있다. ▶좌장 : NO는 아주 불안정하고 반감기도 매우 짧은 물질이다. NO를 안정화시킬 수 있는 방법이 무엇인가? ▶Ignarro : 많은 학자와 제약회사들이 이 문제로 난관에 부딪혔다. 고농도의 NO를 세포에 도달할 수 있을 정도로 안정화하기가 매우 어렵다. Nebivolol은 NO를 공급하는 약(NO donor drug)이 아니라 NO synthase를 활성화시켜 세포가 스스로 NO를 생산하게 만드는 약이다. Nitroglycerin 역시 평활근에서 NO로 대사되는 것이지 NO donor drug이 아니다. NO 안정화에 대해 많은 고민을 했지만 아직 해결책을 찾지 못했다. 단지 실험을 통해 특정 antioxidant가 있으면 NO가 안정화돼 반감기가 최소 수 초 정도 증가하는 것을 확인했다. 즉, 환자가 antioxidant나 신선한 채소를 많이 먹어 체내 항산화작용이 활발하면 어떤 약이든 NO의 효과를 높일 수 있지 않을까 추정한다. ▶좌장 : 그런 어려움을 감안할 때, NO의 반감기를 늘린 nebivolol은 획기적인 약제라 생각한다. ▶Ignarro : 맞는 말이다. NO의 반감기를 늘리기는 매우 어렵다. Nebivolol과 같은 약이 필요한 환자들은 보통 비만·당뇨병 등 심혈관 및 동맥 질환을 유발하는 다른 질병을 갖고 있다. 이처럼 산화스트레스(oxidative stress)가 높으면 NO가 부족해지고 내피세포 기능부전(Endothelial Dysfunction)이 발생한다. Nebivolol은 내피세포 기능부전이 있는 환자에서도 임상적 효과가 있는 것으로 확인됐다. Nebivolol은 내피세포에서 NO 생성을 촉진하는 것이다. 내피세포 기능부전이란 NO를 전혀 생산하지 못한다는 뜻이 아니라 NO 생산량이 감소한다는 뜻이다. 따라서 내피세포에서 NO 생성을 촉진하면 장기적으로 내피세포 기능부전도 개선할 수 있다. NO 자체가 antioxidant이고 여러 가지 유익한 효과를 갖고 있는 cGMP를 증가시키기 때문이다. ▶김범석 : 신장내과 전문의로서 NO 과용량의 부작용에 대해 걱정하지 않을 수 없다. NO가 내피세포의 증식을 억제한다고 했는데, 지나치면 내피세포의 생존에 부작용을 미치지는 않는가? ▶Ignarro : 쥐의 대동맥평활근세포(SMC)를 조직배양해 NO를 추가한 결과 세포증식이 억제됐다. 하지만 내피세포를 배양해 NO를 추가한 결과 세포증식이 억제되지 않았고, 일부 실험에서는 NO가 오히려 세포증식을 촉진시키는 것으로 나타났다. 물론 평활근세포와 내피세포가 다르기는 하지만 이 상반된 결과에 대해 아직 어떤 결론을 내리지 못했다. 그런데 인간의 암세포를 조직배양해 NO를 추가한 결과 암세포 증식이 억제되는 것을 발견했다. 그러므로 이에 대해서는 추가 연구가 필요하다. ▶임상현 : Myocardial fibrosis(심근섬유증)와 fibroblast(섬유아세포)에 대한 NO의 효과에 대해 알고 싶다. NO가 세포증식을 억제한다고 했는데, NO의 fibrosis 또는 fibroblast 억제 효과를 실험한 적이 있는가? ▶Ignarro : NO와 fibroblast의 관계에 대한 연구는 아직 없는 것으로 안다. 이 분야에 대해 잘 알지 못해 답하기 어렵다. ▶이해영 : eNOS(endothelial nitric oxide synthase)와 iNOS(Inducible nitric oxide synthase)의 차이를 알고 싶다. eNOS는 염증을 억제하지만 iNOS는 염증을 촉진하는 것으로 알고 있다. ▶Ignarro : 그에 대해 확답을 내릴 수 있는 사람은 없다. eNOS와 iNOS 모두 NO를 생성한다. 염증이 있는 부위에서는 항상 iNOS가 발견된다. 즉, 염증이 iNOS의 합성을 유도한다고 볼 수 있다. 하지만 반대로 iNOS나 NO가 염증을 유발한다고 볼 수는 없다. 어떤 연구자료를 봐도 NO가 염증을 유발한다는 것을 입증한 사례는 없다. NO의 화학적 속성을 보면 NO가 항염증 효과가 있음을 알 수 있다. 염증은 iNOS 합성을 유도하는데 그 외 어떤 결과를 가져오는지 살펴볼 필요가 있다. 염증이 생기면 산화스트레스(oxidative stress)가 증가하고, 조직을 파괴하는 다량의 superoxide, hydrogen peroxide 또는 기타 oxygen radical이 생성된다. 개인적으로 염증에 iNOS가 유도되는 것은 최대한 NO 생산량을 늘려 oxygen radical에 반응하도록 해 항산화효과를 유발하려는 시도가 아닌가 생각한다. iNOS는 다량의 NO를 생성하는데 정확히 염증부위에서 superoxide가 형성되는 위치에 NO를 생성한다. NO는 superoxide와 반응해 peoxinitrite를 만든다. peoxinitrite는 염증을 일으키거나 세포손상을 유발한다는 연구가 있다. NO가 염증을 유발하는지 여부에 대해서는 추가 연구가 필요하다. ▶이해영 : eNOS는 염증을 유발하지는 않는가? ▶Ignarro : eNOS는 유도되는 것이 아니라 생체 내에 항상 존재한다. eNOS는 염증 여부에 관계 없이 소량의 NO를 생산한다. eNOS가 좀더 많은 양의 NO를 생산한다 해도 절대 염증을 유발하지 않는다. ▶하종원 : 건강한 사람과 전신성 자가면역질환(systemic autoimmune diseases) 환자를 비교한 결과 전신성 자가면역질환 환자에서 항상 염증 발생률이 높았다. Ignarro 박사의 설명에 따르면 심각한 염증은 경미한 염증보다 iNOS 생성을 촉진할 수 있고, 이것이 iNOS와 eNOS의 관계 때문이 아닐까 생각한다. 다른 질문으로 운동유도폐동맥고혈압(exercise-induced pulmonary hypertension)에 대해 연구한 결과 여성에서 남성보다 더 흔하게 관찰됐는데, 이와 같은 현상을 일으키는 요인 중 혹시 NO 생성 또는 합성에 있어 성별에 따른 차이가 있는지? ▶Ignarro : 잘 알려져 있듯이 폐경기 전 에스트로겐 레벨이 높은 여성은 남성보다 심혈관질환에 대한 대항력이 더 강하다. 문제는 50세 이상의 폐경기 여성이다. 미국의 경우 에스트로겐대치요법(estrogen replacement therapy)을 실시한 여성 역시 남성보다 심혈관질환에 걸릴 확률이 낮았다. 이후 에스트로겐대치요법의 위험성이 제기돼 이 요법은 더 이상 사용하지 않는다. 현재 적어도 미국에서는 폐경기 여성의 심혈관질환 발병률이 남성보다 높은 것으로 알고 있다. 에스트로겐 수용체가 NO 생성을 촉진하기 때문에 에스트로겐 레벨이 감소하면 NO 생산량도 감소한다. 많은 연구에서 여성의 경우 에스트로겐이 없을 때보다 에스트로겐이 있을 때 내피에서 더 많은 NO가 생성된다고 보고했다. 따라서 단순한 성별이 아니라 에스트로겐을 기준으로 성별에 따라 NO 생성에 차이가 있다고 볼 수 있다. ▶좌장 : NO 기체는 유해한 기체다. NO의 부작용을 걱정하지 않을 수 없다. NO에 어떤 유해성이 있는가? ▶Ignarro : 이 질문에 답하려면 NO의 화학적 속성을 이해할 필요가 있다. NO가 oxidant에 의해 산화되어 독성물질인 NO2가 되기 위해서는 아주 고농도의 NO가 필요하다. iNOS가 인체 내에서 생성하는 NO양의 수만 배에 달하는 NO가 필요하고, eNOS는 아주 미량의 NO만 생산한다. 실험실에서 미량의 NO를 공기 중 산소와 접촉시키면 NO2를 거의 감지할 수 없다. NO2가 되기 전에 NO가 파괴되기 때문이다. iNOS는 인체 내에 다량의 NO를 생성하지만 NO2로 변환된다는 증거는 전혀 없다. NO가 oxidant와 반응하여 peoxinitrite나 다른 분자를 생성하긴 하지만 NO2를 만들지는 않는다. 물론 가스탱크에서 NO를 직접 흡입하면 당연히 문제가 되지만 인체 스스로 NO를 생산하도록 자극했을 때의 부작용은 현재까지 밝혀진 바가 없다. 단, 패혈쇼크(septic shock)가 있는 경우는 예외다. 패혈쇼크 환자의 경우 극도의 혈관확장과 모든 장기의 hypoperfusion(관류저하)가 발생해 치료가 거의 불가능하다. 임상적으로 혈관수축제를 써도 패혈쇼크를 막기 어렵다. 결국 패혈쇼크 환자는 NO로 인해 혈관이 완전히 확장되어 사망하게 된다. 정리하면 패혈쇼크 환자의 경우 NO를 과다하게 생성시키면 hypoperfusion과 혈압강하로 인해 환자는 사망하지만, 일반적인 경우 NO의 부작용은 밝혀진 바가 없다. ▶정해억 : NO는 혈압을 강하시키는데 왜 항고혈압제로 분류되지 않는가? ▶Ignarro : 순수 NO는 기체이기 때문에 알약이나 주사로 주입할 수 없다. 희석시킨다 해도 항고혈압제로 사용하려면 흡입을 해야 한다. 하지만 순환계로 들어가는 즉시 NO는 oxyhemoglobin에 의해 분해·산화돼 비활성화 된다. 따라서 NO는 고혈압 강하제로는 사용할 수 없다. 하지만 NO는 폐혈압(pulmonary blood pressure) 강하에는 흔히 사용된다. 특히 심장이나 폐에 문제가 있는 신생아 등 유아에 많이 사용된다. 즉, 순환되기 전에 NO가 폐에 국부적으로 작용해 신생아를 살리는 것이다. ▶좌장 : NO에 대한 내성은 없는가? ▶Ignarro : Nitroglycerin에는 내성이 생길 수 있다. NO의 효과를 처음 발견했을 때부터 NO 내성에 대해 고민을 했다. NO에 내성이 생기면 내피세포 기능부전을 유발할 수도 있기 때문이다. 하지만 아직까지 NO에 대한 내성을 입증한 연구는 없다. Nitroglycerin에 내성이 생기는 이유는 nitroglycerin을 환자에게 지속적으로 장기 투여하면 nitroglycerin를 NO로 변환시키는 효소를 모두 소모시키기 때문이다. 따라서 투약을 중단하고 효소가 복구될 때까지 기다린 후 다시 nitroglycerin를 투여해야 한다. ▶좌장 : 노벨상 수상자이신 Ignarro 박사를 모시고 학술좌담회를 하게 돼 큰 영광이고, NO와 관련된 비하인드 스토리와 심혈관질환 임상 적용에 대한 명쾌한 강의와 해답을 얻게 돼 큰 기쁨이었다. 오늘 참석해주신 모든 분들에게 감사드린다. |


