영국피부과협회, 2020년 생물학적 제제 건선치료 가이드라인 발표
11개 치료제 효과·내약성, 누적 확률·최선일 확률 수치로 순위 매겨
스카이리치(성분명 리산키주맙)의 국내 급여권 진입이 초읽기에 들어간 가운데 유럽에서 건선 관련 생물학적 제제 전체를 비교한 가이드라인이 나와 눈길을 끈다. 가이드라인에서 스카이리치에 대한 평가는 선발 인터루킨 치료제의 긴장을 부른다.
현재 국내에서는 정부와의 약가협상이 진행 중이지만, 후발약제로서 기존 치료제 대비 높은 약가 요구는 없을 것으로 알려졌다. 스카이리치의 급여 출시는 기존 건선치료제 시장 판도를 흔들 것으로 예상된다.
영국피부과협회(BAD)는 지난 24일(현지시간) '2020년 생물학적 제제 건선치료 가이드라인'을 발표했다.
BAD는 영국 보건부, 영국 국립보건임상연구원(NICE) 및 환자단체 등과 협력해 피부과 진료의 모범사례 및 피부과 의료서비스 제공에 대한 가이드라인을 제공하고 있다.
이번 가이드라인은 2017년 이후 3년 만에 개정된 버전이다. 이 기간 새로운 생물학적 건선 치료제의 개발과 장기임상, 비교임상 등이 진행되면서 결과에 국내외 전문가들의 이목이 쏠려있다.
BAD는 이번 가이드라인에서 11종의 생물학적 건선 치료제에 대한 네트워크 메타분석을 통해 약제별 효과와 안전성을 평가했다.
메타분석 대상 치료제는 TNF 억제제군의 휴미라(아달리무맙)·퍼스티맙(세르톨리주맙 페골)·엔브렐(에타너셉트)·레미케이드(인플릭시맵)와 인터루킨-12/23 억제제 스텔라라(우스테키누맙), 인터루킨-17 억제제 코센틱스(세쿠키누맙)·탈츠(익세키주맙)·킨테움(브로달루맙), 인터루킨-23 억제제 트렘피어(구셀쿠맙)·스카이리치(리산키주맙)·일루미아(틸드라키주맙).
메타분석에는 각 생물학적 제제별 RCT는 물론 코호트 연구, 제제별 헤드투헤드 연구 등에 따른 효과·안전성 비교와 치료 실패·임신·발암 관련 연구 등을 망라해 포함했다..
RCT의 3∼4개월 데이터와 헤드투헤드 데이터, 헤드투헤드가 없는 경우 임상 간 네트워크 연결을 통해 간접적 데이터 비교가 이뤄졌다.
BAD는 3∼4개월 효과를 비교해 전체 중 해당 치료제가 선택될 누적 확률(SUCRA) 수치와 해당치료가 최선일 확률(Pr. Best) 수치로 순위를 책정했다.
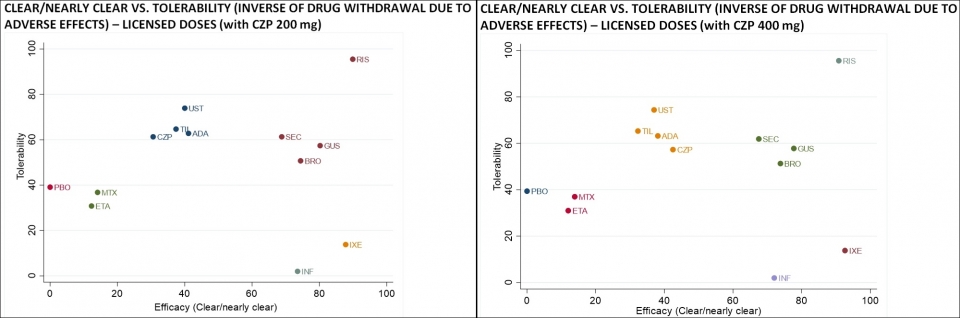
허가된 용량에서의 효과(CLEAR/NEARLY CLEAR)는 퍼스티맙 200mg이 포함된 분석과 400mg이 포함된 분석, 두 가지로 결과가 나왔다.
퍼스티맙은 0·2·4주차에 400mg 투여 후 2주 간격으로 200mg을 쓰거나 효과가 부족할 경우 2주 간격으로 400mg을 쓰도록 허가돼 있기 때문이다.
퍼스티맙 200mg 포함 결과에서 스카이리치는 SUCRA 89.9점, Pr. Best 45.4점으로 11개 생물학적 제제 중 선두를 차지했다. 탈츠가 87.8점·23.4점으로 두번째, 세번째는 트렘피어로 80.2점·14.6점으로 나타났다.
퍼스티맙 400mg 포함 결과에서는 탈츠가 SUCRA 92.6점, Pr. Best 40.5점으로 1등, 스카이리치가 90.8점·37.4점으로 2등, 트렘피어가 77.7점·9.4점으로 3번째에 위치했다.
이 같은 결과는 3∼4개월 PASI 90(건선 피부 90% 개선) 도달률이 영향을 미쳤다. 임상에서 스카이리치는 PASI90 도달률이 74%, 탈츠는 72%, 트렘피어는 68%로 나타났다. 반면 코센틱스는 60%, 스텔라라는 46%에 그쳤다.
내약성에서는 스카이리치가 돋보였다. 이상반응으로 인한 치료중단 등을 살펴본 결과에서 스카이리치는 퍼스티맙 200mg, 400mg 포함 결과와 상관없이 가장 좋은 결과를 냈다.
스카이리치는 두 결과에서 각각 SUCRA 95.5점·95.6점, Pr.Best 78.9점·79.9점을 기록했다. 이는 12주 간격으로 투여하는 스카이리치의 특성이 반영된 것으로 보인다.
같은 12주 간격 투여 치료제인 스텔라라는 SUCRA 73.9점·74.4점, Pr.Best 1.7점·1.8점으로 두번째에 자리했다.
4주 간격으로 1년에 17회 투여하는 탈츠는 내약성에서 SUCRA 13.8점·13.8점, Pr.Best에서는 점수를 얻지 못했다.
내약성 점수는 처방 시 고려해야 할 사항이 작용 인터루킨 별 차이를 보이면서 결과가 엇갈렸다.
인터루킨-17에 작용하는 치료제는 염증성 장질환 및 재발성 칸디다염 등을 처방 시 고려해야 하는 반면 인터루킨-23 치료제는 특별히 고려해야 할 사항이 없었기 때문이다.
이상반응으로 인해 치료를 중단할 확률은 인터루킨 치료제 모두 1∼3%로 낮았으며 심각한 부작용 발생 또한 1% 미만으로 나타났다.
BAD 가이드라인은 국내 처방에도 영향을 미칠 수 있다. 특히 올해 상반기 급여 출시를 목표하고 있는 스카이리치의 경우 호재로 작용할 가능성이 높다.
국내 건선치료제 업계 관계자는 "스카이리치가 후발주자로서 급여권 진입을 서두르고 있다"며 "애브비가 빨리 시장을 차지하기 위해 코센틱스·트렘피어·탈츠 등 기존 치료제 수준으로 약가협상의 결론을 낼 것으로 예상된다"고 전했다.


