심평원 암질환심의위 '급여기준 미설정', 불합격 통지
BMS 백혈병 치료제 '스프라이셀'은 급여 확대 청신호

식품의약품안전처 신속심사를 통해 국내 처음으로 RET 표적치료제로 허가받은 '레테브모(성분명 셀퍼카티닙·한국릴리)'가 내친 김에 급여 진입까지 속도를 내봤지만 무위에 그쳤다.
건강보험심사평가원은 5월 18일 암질환심의위원회를 열고 레테브모 급여기준을 심의한 결과, 관련 급여 기준을 설정하지 않는 것으로 결론을 내렸다고 밝혔다. 급여 첫 관문인 암질심 통과 불발, 불합격 통지다.
레테브모는 지난 3월 ▲전이성 RET 융합-양성 비소세포폐암 성인 환자 ▲전신요법을 요하는 진행성 또는 전이성 RET-변이 갑상선 수질암이 있는 성인 및 만 12세 이상 소아 환자 ▲방사선 요오드에 불응하고, 이전 소라페닙 및/또는 렌바티닙의 치료 경험이 있으며 전신요법을 요하는 진행성 또는 전이성 RET 융합-양성 갑상선암 성인 환자 치료제로 식약처 허가를 받은 바 있다.
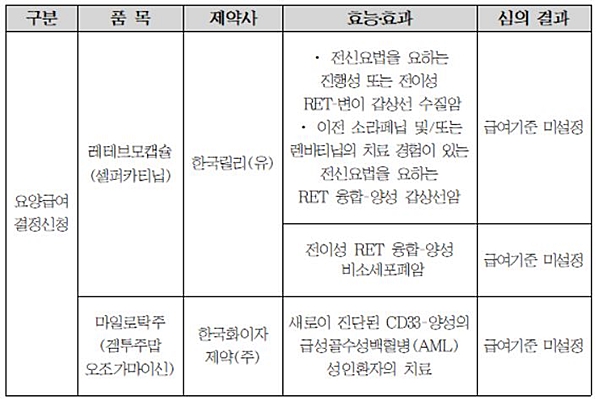
릴리는 이에 기반해 △전이성 RET 융합-양성 비소세포폐암 △전신요법을 요하는 진행성 또는 전이성 RET-변이 갑상선 수질암 이전 소라페닙 및/또는 렌바티닙의 치료 경험이 있는 전신요법을 요하는 RET 융합-양성 갑상선암에 대해 급여 적용을 신청했는데, 암질심은 이들 모두에 대해 불합격 결정을 내렸다.
한국화이자제약의 백혈병치료제 '마일로탁(겜투주맙오조가마이신)' 또한 급여 첫 관문에서 고배를 마셨다. 새로 진단된 CD33-양성의 급성골수성백혈병(AML) 성인환자의 치료제로 마일로탁의 급여 등재를 신청했으나, 급여기준을 설정받지 못해 다음 기회를 기약하게 됐다.

한국BMS제약의 백혈병치료제 '스프라이셀(다시티닙)'은 급여 확대를 위한 첫 발을 뗐다. 새로이 진단받은 만 1세 이상의 필라델피아 염색체 양성 급성 림프구성 백혈병(Ph+ ALL) 소아환자에서 항암화학요법과의 병용요법에 대해서다.
한국노바티스는 골수섬유화증 중간위험군 또는 고위험군 골수섬유화증의 치료제로 '자카비(룩소리티닙)'의 급여 확대를 시도했으나, 불발에 그쳤다.


